Dr. Michael Palmer
Este artículo resume el modo de acción de las vacunas de ARNm, así como tres posibles mecanismos patogénicos que pueden explicar la toxicidad observada con las vacunas de ARNm contra el COVID-19, a saber: toxicidad química de las nanopartículas lipídicas, toxicidad directa de la proteína espiga, cuya la expresión es inducida por las vacunas y los efectos destructivos de la respuesta inmunitaria a la proteína espiga. Se argumenta que, de estos mecanismos, el tercero es probablemente el más importante. Si esta conclusión es correcta, entonces se debe esperar esencialmente el mismo nivel de toxicidad con futuras vacunas de ARNm contra cualquier otro microbio patógeno.
1. Cómo las vacunas de ARNm provocan un ataque inmunitario en nuestras propias células y tejidos
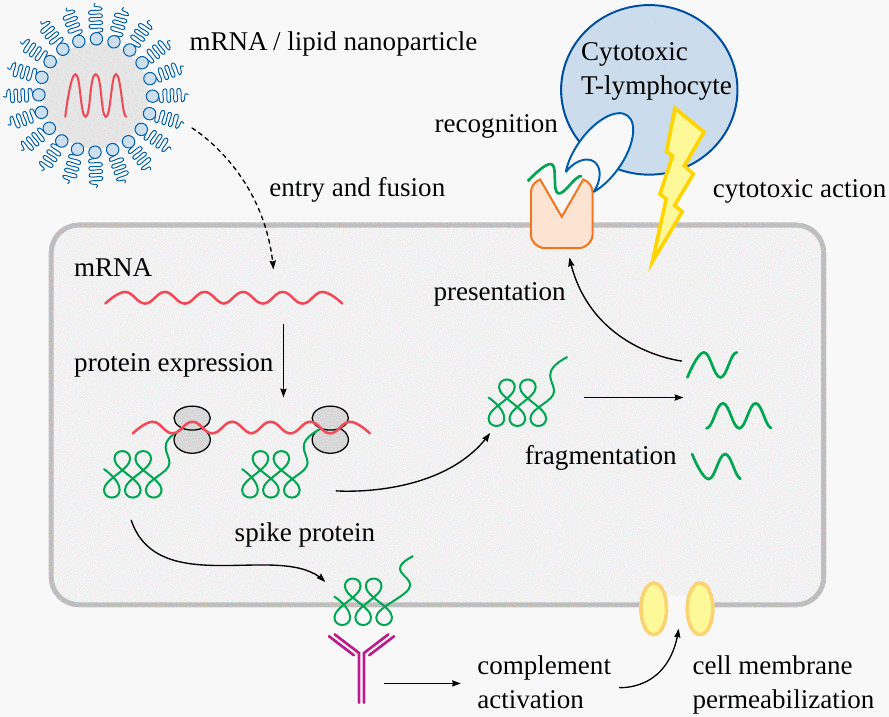
Las partículas de la vacuna de ARNm tienen dos componentes: el propio ARNm y la mezcla de lípidos que lo encierra. Los lípidos protegen al ARNm en tránsito y facilitan su captación celular.
Una vez dentro de la célula, el ARNm se une a los ribosomas, las pequeñas manchas grises en la caricatura, que leen la secuencia del ARNm y ensamblan la proteína en consecuencia. En el caso de las vacunas COVID-19, el producto es la proteína espiga del virus SARS-CoV-2.
La proteína de punta se llevará a la superficie celular, donde puede unirse a los anticuerpos. Esos anticuerpos unidos activarán el sistema del complemento , una cascada de proteínas séricas que culmina en la formación de un complejo de ataque a la membrana . Dichos complejos crean grandes agujeros en la membrana celular y, en última instancia, matan a la célula.
Otro camino hacia el ataque inmunológico comienza con la fragmentación de algunas moléculas de proteína de pico dentro de la célula. Los fragmentos se llevan de nuevo a la superficie celular, donde son reconocidos por los linfocitos T citotóxicos (células T-killer). El reconocimiento hace que ataquen y maten a la célula infectada.
Lo anterior supone que ya tenemos anticuerpos que reconocen la proteína espiga o sus fragmentos. ¿Cómo surgen estos en primer lugar? Sin entrar en detalles, notamos que su inducción requiere cierta medida de daño celular y muerte celular, provocada, por ejemplo, por las células T-killer. Luego, la respuesta de anticuerpos es inducida por los restos de esas células muertas.
1.1. Claro, eso se ve bastante mal, pero ¿no son las vacunas de ARNm como las vacunas de virus vivos?
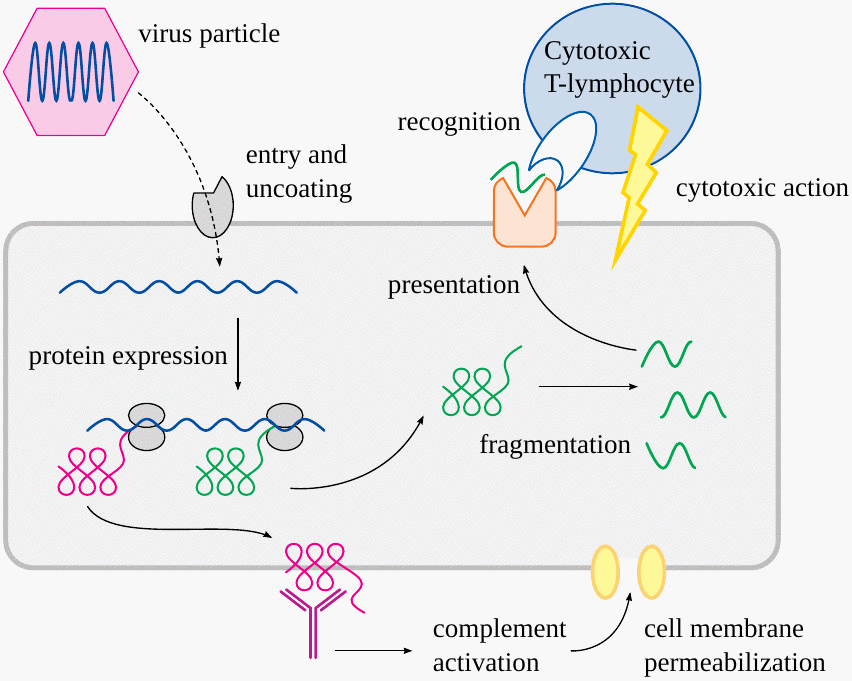
Es cierto que las mismas dos vías también operan en la defensa inmunológica frente a virus naturales y vacunas de virus vivos. Sin embargo, el diablo está en los detalles.
1.2. Tres diferencias clave entre las vacunas de virus vivos y las vacunas de ARNm
| vacunas de virus vivos | vacunas de ARNm | |
| Replicación dentro de la célula huésped | Sí | No |
| Las partículas de la vacuna contienen antígenos proteicos | Sí | No |
| Las partículas de la vacuna infectan las paredes de los vasos sanguíneos | No | Sí |
Veremos ahora por qué estas tres diferencias son importantes.
1.3. El curso temporal de la carga viral y la respuesta inmune en una infección por virus o vacunación con virus vivo
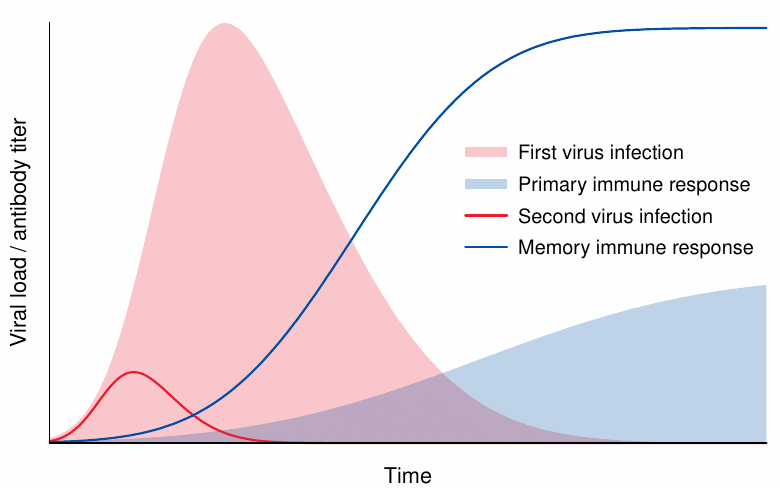
Si nos infectamos con un virus natural o nos inoculan una vacuna de virus vivos, la carga viral inicial es pequeña. En ausencia de inmunidad previa, el virus se replicará durante un buen tiempo y la carga viral aumentará hasta que sea controlada por el inicio de la respuesta inmune. Para cuando la respuesta inmunitaria alcance su punto máximo, la carga viral normalmente ya habrá disminuido y la lucha contra la infección estará en la etapa de «limpieza».
Una infección secundaria desencadenará una respuesta de memoria, que frena la multiplicación del virus desde el principio. Por lo tanto, el pico de la carga viral seguirá siendo mucho más bajo y, a menudo, la infección ni siquiera será clínicamente aparente: somos «inmunes» a ella. Nuevamente, cualquier infección a pequeña escala que ocurra desaparecerá en gran medida para cuando la respuesta inmunitaria alcance su punto máximo. Por lo tanto, ni con la infección primaria ni con una secundaria chocarán frontalmente la carga viral máxima y la respuesta inmunitaria máxima. Esto limita la intensidad de la inflamación.
1.4. Las inyecciones repetidas de vacunas de ARNm chocarán con la inmunidad existente
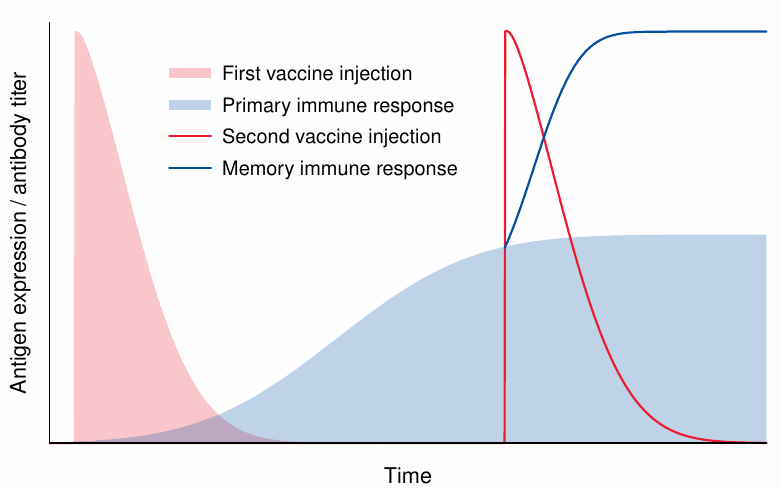
Ahora llegamos a la primera disparidad entre los virus y las vacunas de ARNm, a saber, que, a diferencia de los virus, las vacunas de ARNm no se replican. Esto hace que sea necesario inyectar la cantidad total de partículas de vacuna de una vez y cada vez.
Se supone que la expresión del antígeno declina en una escala de tiempo de días. Si asumimos que este es el caso, y también que aún no existe inmunidad, podemos evitar nuevamente un choque entre la expresión máxima del antígeno y la respuesta inmune máxima. Sin embargo, con una inyección repetida, y también en caso de inmunidad natural debido a una infección previa con el virus, debemos esperar que la expresión del antígeno choque de frente con una respuesta inmune intensa, lo que resulta en una inflamación intensa en consecuencia. Por lo tanto, tanto los efectos secundarios agudos como los a largo plazo, como los trastornos autoinmunes, serán más probables después de la segunda inyección.
1.5. A diferencia de los virus, los anticuerpos no reconocen las partículas de la vacuna de ARNm
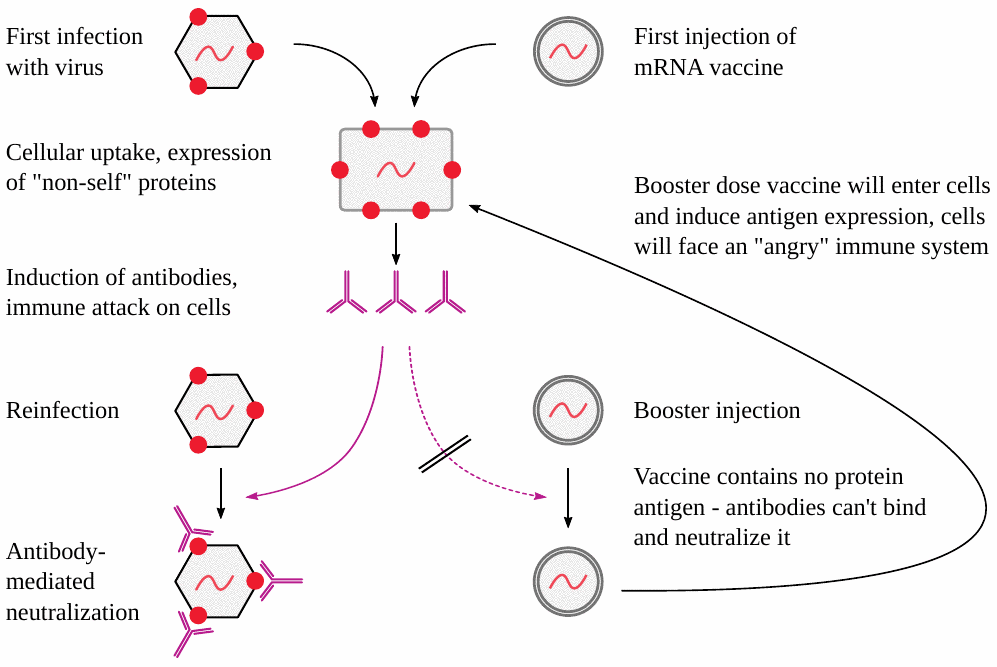
La preocupación por el choque frontal entre la expresión del antígeno de la vacuna y la respuesta inmune se ve agravada por la segunda disparidad entre los virus y las vacunas de ARNm, a saber, que las partículas de la vacuna de ARNm no contienen ninguna copia del antígeno proteico codificado en sus superficies.
La presencia de antígenos de proteínas en partículas de virus significa que estos pueden unirse a anticuerpos que ya están presentes, lo que evitará que esas partículas de virus infecten las células de nuestro cuerpo. Aunque algunas partículas todavía pueden pasar, los anticuerpos al menos mitigarán la infección.
En contraste, las partículas de la vacuna de ARNm no pueden ser detenidas por los anticuerpos en absoluto, por la sencilla razón de que contienen solo el modelo de ácido nucleico para la proteína, pero no la proteína en sí. Por lo tanto, estas partículas serán absorbidas por las células de nuestro cuerpo independientemente de la inmunidad. Cualquier inmunidad ya presente se dirigirá entonces contra esas desafortunadas células.
Por lo tanto, en pocas palabras, con los virus reales, la inmunidad existente inhibirá el daño celular y la inflamación, mientras que con las vacunas de ARNm, la inmunidad existente empeorará las cosas.
1.6. Resumen: los defectos inherentes de las vacunas de ARNm
- La alta carga de partículas choca con una respuesta inmune intensa
- Las partículas «vuelan por debajo del radar» de la vigilancia de anticuerpos antes de ingresar a las células, dirigiendo un sistema inmunitario «enojado» contra esas células
- La expresión de antígenos en las células de las paredes de los vasos sanguíneos provoca la destrucción de los vasos, con activación de la coagulación de la sangre.
Los dos primeros puntos promueven una inflamación intensa, con destrucción tisular severa y riesgo de desencadenar autoinmunidad. El daño a los vasos sanguíneos también presenta riesgos graves; esto se ilustra con la grave enfermedad causada por esos virus naturales que infectan las paredes de los vasos sanguíneos. Algunos ejemplos son los virus Ébola, Marburg y Dengue.
2. Gravedad del evento adverso después de la inyección repetida de la vacuna
2.1. Mayor gravedad de los eventos adversos en adolescentes después de la segunda inyección de la vacuna Moderna
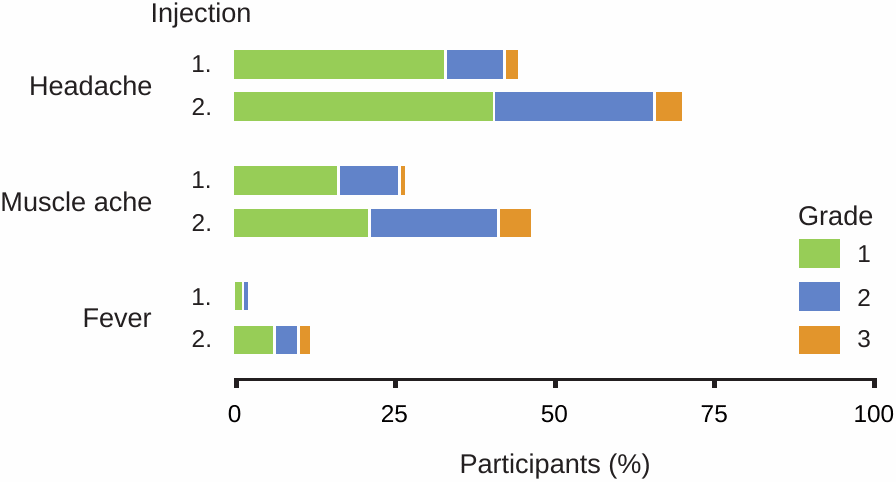
Esta figura está adaptada de Ali et al. [ 1 ] , el “ensayo clínico” de la vacuna Moderna en adolescentes. Vemos un aumento general en la gravedad después de la segunda inyección, particularmente con efectos secundarios de grado 2 y 3. Fiebre de grado 3 significa entre 39 y 40 grados centígrados. Una fiebre tan alta indica un potencial de inflamación grave y normalmente se considera inaceptable en una vacuna candidata.
2.2. Síntomas cardíacos en adolescentes después de la primera y segunda inyecciones con la vacuna de Pfizer
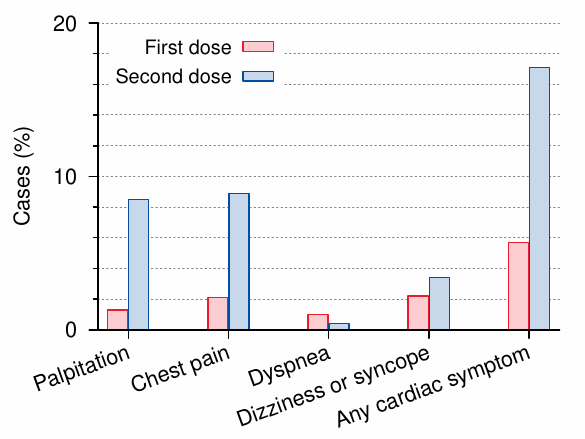
Los datos de esta figura son de Chiu et al. [ 2 ] , que siguió a aproximadamente 5000 adolescentes inyectados. Vemos una incidencia claramente mayor de síntomas después de la segunda inyección.
Los síntomas cardíacos monitoreados en este estudio son comparativamente «leves», pero son muy frecuentes, lo que nos lleva a esperar que también ocurran consecuencias cardíacas más graves. Muchos de estos vacunados sintomáticos probablemente sufrieron algún grado de inflamación en el corazón.
2.3. Informes VAERS de miocarditis después de la primera y la segunda dosis
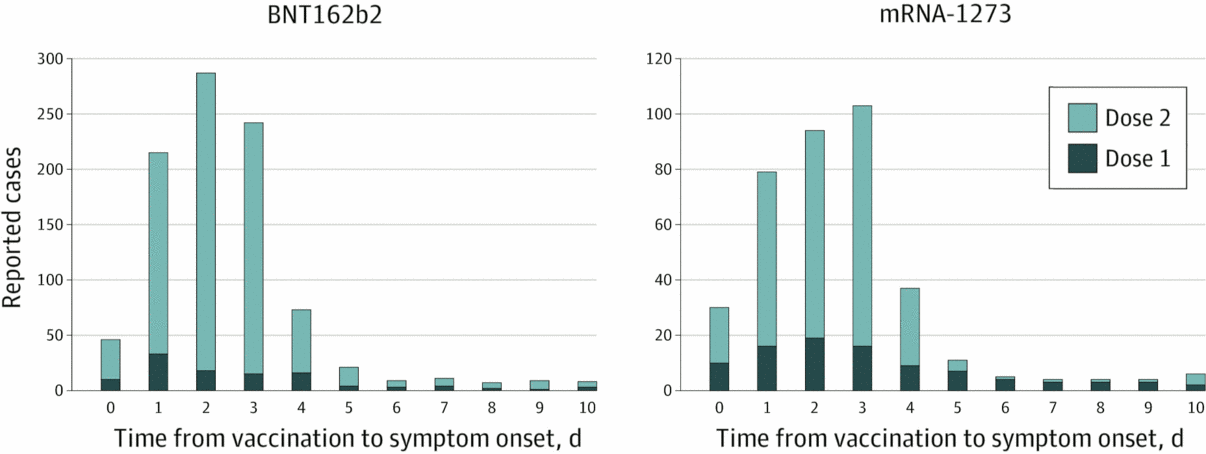
Por supuesto, ya sabemos que la miocarditis inducida por vacunas no es rara. Esta figura (adaptada de Oster et al. [ 3 ] ) muestra que con la miocarditis, también, la incidencia es significativamente mayor después de la segunda inyección que la primera. Un estudio de Basilea en Suiza sugiere una incidencia aún mayor después de la tercera inyección [ 4 ] .
2.4. Días hasta la muerte por edad y dosis (VAERS, hasta 2021-11-23)
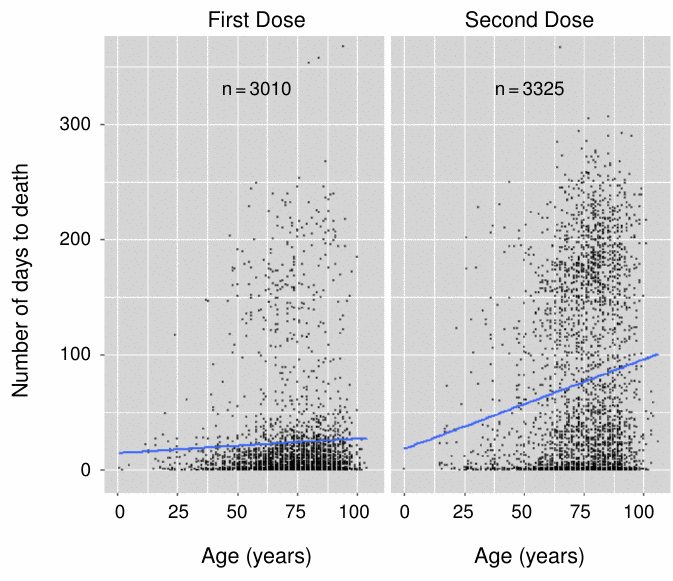
Este análisis, realizado por Craig Pardekooper de la fama de “Qué malo es mi lote” [ 5 ] , sugiere que la historia es un poco más complicada. Aparentemente, hay más muertes tardías, pero menos tempranas después de la segunda dosis.
Los números totales de muertes en ambos paneles son bastante similares. Sin embargo, es lógico pensar que la probabilidad de que se establezca una conexión entre una inyección y una muerte u otro evento adverso grave disminuye con el tiempo; o en otras palabras, que el sesgo de subregistro aumentará con el tiempo. Por lo tanto, es probable que las muertes tardías estén subrepresentadas en relación con las tempranas. Esto sugiere que la mortalidad general será significativamente mayor después de la segunda dosis.
3. Mecanismos alternativos de daño por vacunas
- Toxicidad química de las nanopartículas lipídicas
- Toxicidad de proteína de pico
- Respuesta inmune a la proteína espiga como antígeno extraño
- Inducción de mutaciones genéticas por el ARNm y por el ADN contaminante
A continuación, veremos brevemente los primeros tres mecanismos y luego consideraremos cuál es el más probable predominante. El cuarto mecanismo fue discutido en un artículo anterior [ 6 ] .
3.1. Los lípidos catiónicos son altamente inflamatorios.

Esta figura está adaptada de un artículo de Ndeupen et al. [ 7 ] , que inyectó a los ratones mezclas de lípidos similares a las utilizadas en las vacunas de ARNm de la COVID-19. El panel de la izquierda muestra parches de piel extirpados de ratones a los que se les había inyectado tampón (PBS) solamente, con una mezcla de lípidos inertes (nNLP) o con una mezcla de lípidos que contenía lípidos catiónicos (iLNP). En este último caso, los parches de piel están inyectados en sangre, lo que indica inflamación. Los gráficos de la derecha muestran que las células inflamatorias, en particular los granulocitos de neutrófilos, también aumentan en este caso.
3.2. Los lípidos catiónicos inducen especies reactivas de oxígeno, que pueden inducir la apoptosis (muerte celular programada)

Los lípidos catiónicos también pueden inducir la muerte celular programada (apoptosis), que puede detectarse mediante la fragmentación del ADN, como se muestra en este experimento de electroforesis. Los fragmentos de ADN se separan aquí según el tamaño: cuanto más lejos del origen a la izquierda, más pequeños son. En cultivos celulares, este efecto se puede suprimir mediante la adición de un agente reductor (N-acetilcisteína), lo que indica que está mediado por especies reactivas de oxígeno (ROS).
La inducción de ROS por lípidos catiónicos se ha confirmado en múltiples estudios y presenta un riesgo de daño en el ADN incluso si no se alcanza el umbral de apoptosis total. Este riesgo está respaldado por algunos datos muy fragmentarios sobre el daño genético en los precursores de glóbulos rojos, que Moderna presentó a la Agencia Europea de Medicamentos [ 8 ] .
3.3. Actividades tóxicas de la proteína espiga
- El fragmento de proteína espiga S1 se puede separar de las superficies celulares y entrar en el torrente sanguíneo
- El fragmento S1 se une e inhibe la enzima convertidora de angiotensina (ACE2)
- El sustrato de ACE2, la angiotensina II, se acumula y provoca
- presión sanguínea elevada
- activación de la coagulación de la sangre
- aumento de la inflamación
- La proteína de pico intracelular inhibe la reparación del ADN
La proteína espiga en sí también tiene actividad tóxica, que puede estar mediada por la inhibición de ACE2 [ 9 , 10 ] y, potencialmente, también por la inhibición de la reparación del ADN [ 11 ] , lo que puede agravar los riesgos mutagénicos que plantea el ARN y el ADN contaminante [ 6] . ] así como los lípidos catiónicos.
3.4. Patología inmune después de la vacunación («linfocitos amok»)

Esta diapositiva muestra el tejido del músculo cardíaco normal a modo de comparación y el tejido del músculo cardíaco afectado por la miocarditis inducida por la vacuna, como se desprende del grupo de linfocitos en el medio. Esta imagen es de un caso de autopsia informado por el patólogo Prof. Arne Burkhardt, quien usó el término «linfocitos locos» para resumir sus hallazgos en muchos órganos y en muchos pacientes que murieron después de recibir vacunas COVID-19 basadas en genes.
3.5. Tejido pulmonar sano y grupos de linfocitos en el pulmón de una víctima de la vacuna

Esta imagen, también del Prof. Burkhardt, muestra una inflamación linfocítica del pulmón. Los tabiques alveolares normalmente delicados del tejido pulmonar están engrosados por tejido cicatricial y los espacios llenos de aire (blancos) están comprimidos.
Los puntos azul oscuro en el panel izquierdo son los núcleos celulares de las células regulares dentro del tejido. Algunos de los puntos azules en el panel derecho son de la misma naturaleza. Sin embargo, el grupo grande dentro del cuadrante superior izquierdo es una acumulación de linfocitos invasores.
3.6. Vasculitis de pequeños vasos sanguíneos en el cerebro
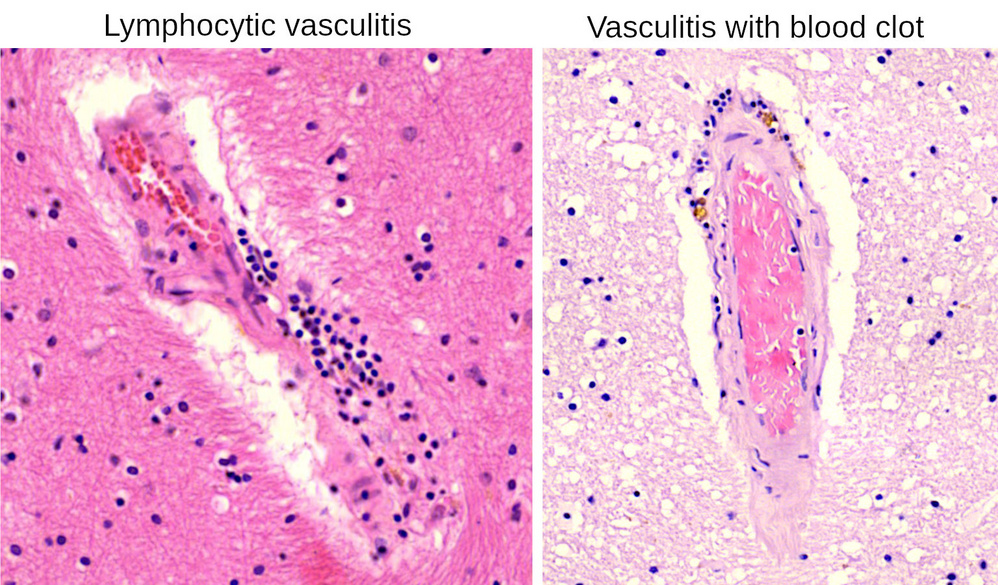
Los vasos sanguíneos de todos los tamaños se ven afectados de manera prominente por la inflamación linfocítica. Esta diapositiva (nuevamente del Prof. Burkhardt) muestra dos pequeños vasos inflamados dentro del tejido cerebral. A la derecha, las lesiones inflamatorias han provocado la coagulación de la sangre dentro del vaso.
También se observan linfocitos en el propio tejido cerebral circundante, lo que indica que la inflamación no se limita a los vasos sanguíneos.
3.7. Expresión de proteína de pico en un caso de encefalitis inducida por vacuna
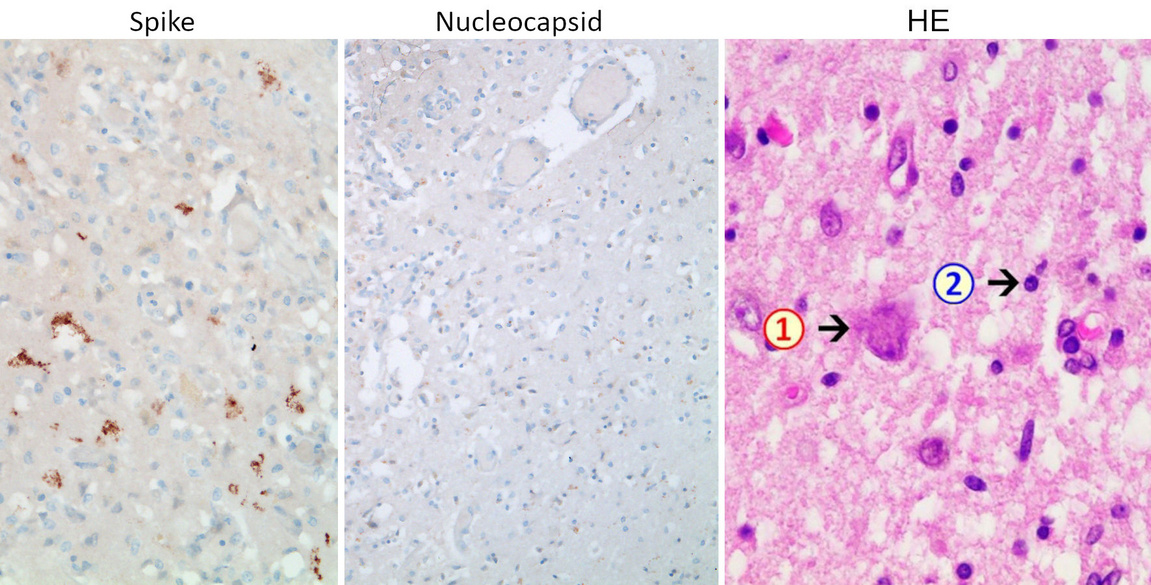
La conexión causal entre la inyección de la vacuna y la inflamación puede demostrarse mediante inmunohistoquímica. En este método, la especificidad de los anticuerpos para una determinada proteína de interés, como en nuestro caso la proteína espiga, se utiliza para su detección sensible y selectiva en secciones de tejido. Varios pasos después de la unión del anticuerpo, se genera un pigmento marrón que muestra la presencia y distribución de la proteína objetivo.
Esta diapositiva muestra secciones del cerebro de un paciente que murió varias semanas después de recibir su inyección de vacuna COVID-19 más reciente [ 12 ] . La tinción convencional (HE) de la derecha muestra una célula nerviosa muerta (1) y células inflamatorias que incluyen linfocitos (2). El diagnóstico realizado fue encefalitis necrotizante, es decir, inflamación del cerebro con muerte celular/tejida.
En el panel izquierdo, vemos que varias células expresan la proteína de punta en una muestra de tejido cerebral, como lo demuestra la deposición de pigmento marrón sobre esas células. El panel central muestra que la nucleocápside , otra proteína del virus SARS-CoV-2, no se expresa. La vacuna codifica solo la espiga, mientras que las células infectadas por el virus deben expresar todas las proteínas virales, incluida también la nucleocápside. Por lo tanto, la proteína del pico que se detecta debe haber sido inducida por la vacuna. Esto encaja con la historia clínica de este caso, que incluía tres vacunas pero ningún diagnóstico de infección por el virus.
3.8. Miocarditis con depósitos de complemento e infiltrados principalmente granulocíticos
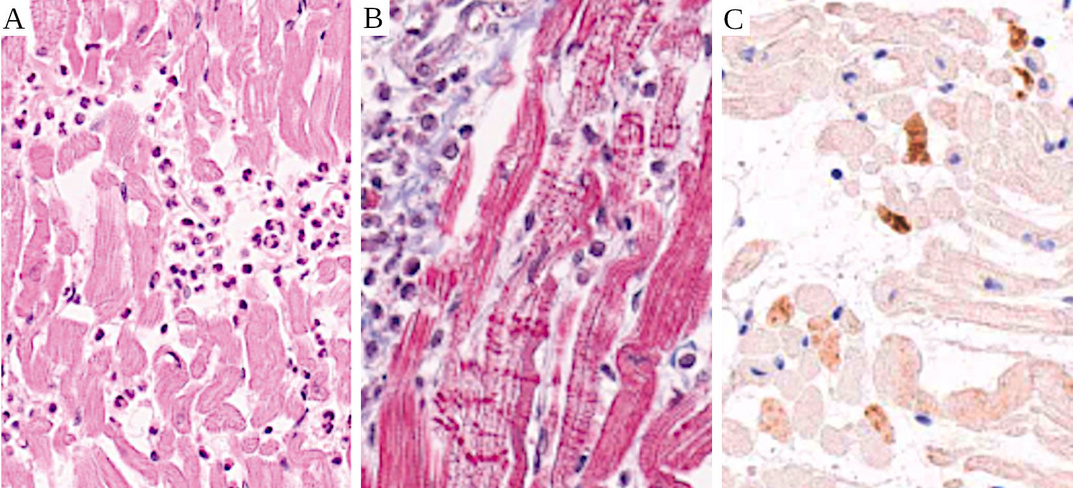
Este caso de miocarditis con muerte súbita fue informado por Choi et al. [ 13 ] . Cinco días después de la primera dosis de la vacuna de Pfizer, el paciente desarrolló dolor en el pecho y murió siete horas después. Los depósitos de factor C4 del complemento se muestran mediante inmunohistoquímica en el panel C. Se observan infiltrados celulares predominantemente con granulocitos neutrófilos en los paneles A y B. Las franjas rojas horizontales en el panel B son necrosis en bandas de contracción, que se sabe que ocurren después de un exceso de calcio intracelular.
La activación del complemento dará como resultado la permeabilización de la membrana (consulte la Sección 1 ), lo que explica el exceso de calcio y la necrosis de la banda de contracción. La activación del complemento también liberará factores quimiotácticos que atraerán granulocitos a la escena. Este caso, por lo tanto, ejemplifica la ruta mediada por anticuerpo/complemento del ataque inmunitario a las células que expresan el antígeno codificado por la vacuna de ARNm. Lo más probable es que el desafortunado paciente ya tuviera una fuerte inmunidad natural al virus SARS-CoV-2.
4. ¿Cuál de los tres mecanismos es el dominante?
| Mecanismo | Efecto esperado de la segunda dosis | Comentario |
| Toxicidad de lípidos | ningún cambio | toxicidad de las vacunas basadas en adenovirus? |
| Toxicidad directa de la proteína del pico | reducido | responsable de los efectos rápidos de la primera dosis? |
| Respuesta inmune a la proteína de pico | aumentó | completamente general: debe esperarse con todas las futuras vacunas de ARNm |
Una consideración clave para identificar el mecanismo dominante de la toxicidad de la vacuna de ARNm es cómo debe cambiar la intensidad de cada uno de ellos con la segunda inyección.
Con los lípidos catiónicos, uno podría esperar niveles similares de toxicidad aguda después de cada aplicación, aunque es concebible cierto grado de toxicidad aguda acumulativa. Sin embargo, observamos que el espectro de eventos adversos observados con las vacunas COVID-19 basadas en adenovirus es muy similar al de las vacunas de ARNm, aunque las vacunas basadas en virus no contienen lípidos catiónicos. Este hallazgo sugiere que el principio tóxico común de ambos tipos de vacunas es la proteína de pico, ya sea su toxicidad directa o la respuesta inmune a ella.
La toxicidad directa de la proteína espiga debe mitigarse con anticuerpos específicos contra ella, del mismo modo que la difteria y el tétanos se mitigan con anticuerpos contra sus respectivas toxinas proteicas. Por lo tanto, debemos esperar que los anticuerpos inducidos por la primera inyección de vacuna reduzcan la gravedad de los eventos adversos que siguen a la segunda inyección. Sin embargo, como se indica en la Sección 2 , la gravedad de los efectos secundarios tiende a aumentar con la aplicación repetida de la vacuna. La única excepción fueron las muertes prematuras, que de hecho fueron más frecuentes después de la primera inyección que de la segunda (ver Sección 2.4) .). Craig Pardekooper también encontró la misma tendencia con eventos adversos no mortales. Parece posible, por lo tanto, que muchos eventos adversos que ocurren poco tiempo después de la primera inyección estén relacionados con la toxicidad directa de la proteína espiga, que se manifiesta en la ventana de tiempo entre la inyección y la inducción de anticuerpos.
Los siguientes argumentos respaldan un papel clave de la respuesta inmunitaria a la proteína espiga:
- se sigue de las consideraciones teóricas detalladas en la Sección 1 ;
- concuerda con la tendencia predominante de mayor incidencia y gravedad de eventos adversos después de la inyección repetida de la vacuna;
- explica los hallazgos histopatológicos de inflamación intensa e infiltración con linfocitos y otras células inmunitarias, que se observan cerca de los focos de expresión de proteína de punta.
¿Por qué importa cuál de los mecanismos patogénicos es predominante? Hay planes para convertir las vacunas existentes, incluidas las vacunas infantiles, a tecnología de ARNm. Si la toxicidad directa de la proteína de punta del SARS-CoV-2 fuera la principal responsable de los eventos adversos causados por las vacunas de ARNm de COVID-19, entonces las futuras vacunas de ARNm podrían ser más benignas, siempre que las proteínas antigénicas que codifican sean menos tóxicas que la proteína del pico SARS-CoV-2.
Por otro lado, cada vacuna de ARNm inducirá una respuesta inmune de la misma manera que las vacunas de ARNm de COVID-19. Por lo tanto, si esa respuesta inmune fuera la principal responsable de la toxicidad, entonces debemos esperar resultados catastróficos similares con todas las futuras vacunas de ARNm. Los argumentos presentados en este estudio indican que este es el caso más probable.
Las contribuciones de los otros dos mecanismos no pueden ser ignoradas. La toxicidad directa parece contribuir significativamente a la toxicidad temprana después de la primera inyección. La toxicidad de los lípidos catiónicos tampoco puede descartarse por las siguientes razones:
- casi no se realizaron estudios de seguridad de estas sustancias durante los disfuncionales procesos de aprobación de las vacunas contra el COVID-19, pero los rudimentarios que se realizaron dieron claros indicios de toxicidad;
- la inducción de especies reactivas de oxígeno (ROS) por lípidos catiónicos causará daño en el ADN. Este daño permanecerá incluso después de que se hayan eliminado los lípidos, lo que significa que la toxicidad será acumulativa;
- dado que los lípidos catiónicos son un ingrediente necesario de todas las vacunas de ARNm, su toxicidad se acumulará en todas las dosis de todas las vacunas de ARNm, en lugar de solo en todas las dosis de una sola.
En conclusión, toda la evidencia indica que los tres mecanismos de toxicidad deben tomarse en serio. Al mismo tiempo, apunta a un papel clave de la toxicidad inmunomediada, que resulta de las fallas fundamentales de la tecnología de vacunas de ARNm y debe esperarse que ocurra con futuras vacunas de ARNm dirigidas contra todos y cada uno de los virus u otros microbios patógenos.
Referencias
- (2021) Evaluación de la vacuna mRNA-1273 SARS-CoV-2 en adolescentes . N. ingl. J.Med. DOI:10.1056/NEJMoa2109522
- (2023) Cambios en los parámetros de ECG después de la vacuna BNT162b2 en estudiantes de secundaria . EUR. J. Pediatría. 182:1155-1162
- (2022) Casos de miocarditis informados después de la vacunación COVID-19 basada en ARNm en los EE. UU. Desde diciembre de 2020 hasta agosto de 2021 . JAMA 327:331-340
- (2022) Incidencia significativa de miocarditis después de la tercera dosis de la vacuna de ARN mensajero anti-COVID 19 .
- (2023) ¿Qué tan malo es mi lote? Códigos de lote y muertes, discapacidades y enfermedades asociadas para las vacunas Covid 19 .
- (2023) Las vacunas de ARNm de COVID-19 contienen cantidades excesivas de ADN bacteriano: evidencia e implicaciones .
- (2021) El componente de nanopartículas lipídicas de la plataforma mRNA-LNP utilizado en estudios preclínicos de vacunas es altamente inflamatorio . iCiencia 24:103479
- (2021) Informe de evaluación de la EMA: COVID-19 Vaccine Moderna .
- (2021) Una descripción general de los protocolos MATH+, I-MASK+ e I-RECOVER (una guía para el manejo de COVID-19) .
- (2022) COVID-19, vacunas y deficiencia de ACE 2 y otras angiotensinasas. Cerrando el ciclo del “efecto Spike” . EUR. J. Pasante. Medicina. 103:23-28
- (2021) El pico de SARS-CoV-2 perjudica la reparación de daños en el ADN e inhibe la recombinación de V(D)J in vitro . Virus 13:2056
- (2022) Informe de un caso: encefalitis necrosante multifocal y miocarditis después de la vacunación con ARNm BNT162b2 contra Covid-19 . Vacunas 10:2022060308
- (2021) Muerte súbita inducida por miocarditis después de la vacunación con ARNm de BNT162b2 contra la COVID-19 en Corea: Informe de caso centrado en los hallazgos histopatológicos . J. Korean Med. ciencia 36: e286
Este artículo fue publicado originalmente en https://doctors4covidethics.org/. Lea el original.
